
日前,由南方科技大学化学系副教授田瑞军课题组主导,化学系助理教授李鹏飞课题组、生物系助理教授孙颖课题组参与合作的项目在化学蛋白质组学研究领域取得研究进展,相关成果发表在国际著名综合性学术杂志《美国国家科学院院刊》(Proceedings of the National Academy of Sciences,PNAS),论文题目为“Photoaffinity-engineered protein scaffold for systematically exploring native phosphotyrosine signaling complexes in tumor samples”。这一研究工作主要由田瑞军课题组博士后初碧珠和研究助理何岸(共同第一作者)完成,南方科技大学化学系为第一研究单位,田瑞军、李鹏飞和孙颖为共同通讯作者。

田瑞军、李鹏飞、孙颖合照
田瑞军现任中国蛋白质组组织CNHUPO常务理事、中国质谱学会理事、中国色谱学会理事和中国分子系统生物学学会理事。研究领域主要涵盖生物分析化学、化学蛋白质组学、临床质谱分析和癌症信号转导研究等。
据了解,蛋白质是人体中最主要的物质组成。除了作为构筑生命的基石,人体细胞内的蛋白质在任何时刻都发生着十万种以上的相互作用。这些数量庞大的相互作用将蛋白质组装成种类繁多、功能各异的蛋白质复合物,执行和调控着几乎所有的生命过程和功能。通过超过200种蛋白质翻译后修饰的精准调控,蛋白质复合物具有时空动态变化的特征。以丰度极低的酪氨酸磷酸化为例,其复合物由Src homology 2(SH2)结构域识别和组装,并受到酪氨酸激酶和磷酸酶的精准动态调控,是癌症等重大疾病的重要分子调控机制。以格列卫(Gleevac)为例的众多抗癌药物均以此类蛋白质为靶点。针对酪氨酸磷酸化蛋白质复合物的蛋白质组学研究一直是基础生物学领域的研究热点,但长期以来受到蛋白间结合力弱和存在于难溶的细胞膜附近等技术问题的困扰,很难实现在肿瘤等临床样品中的在体系统表征。
化学蛋白质组学是一门有机地结合化学生物学技术和蛋白质组学分析技术的新兴学科,可实现重要药物靶点及生物标志物的活体及在体标记和规模化分析。本项研究发展了一种化学蛋白质组学技术来克服上述挑战,并将其命名为Photo-pTyr-scaffold。该技术巧妙地通过含有三种功能基团的化学探针为SH2结构域引入光反应基团和富集基团,可实现蛋白质复合物的共价键偶联和亲和富集,从而显著地提高了人或动物组织样本具有动态、弱相互作用力特征的酪氨酸磷酸化蛋白复合物的富集和鉴定能力(图1)。
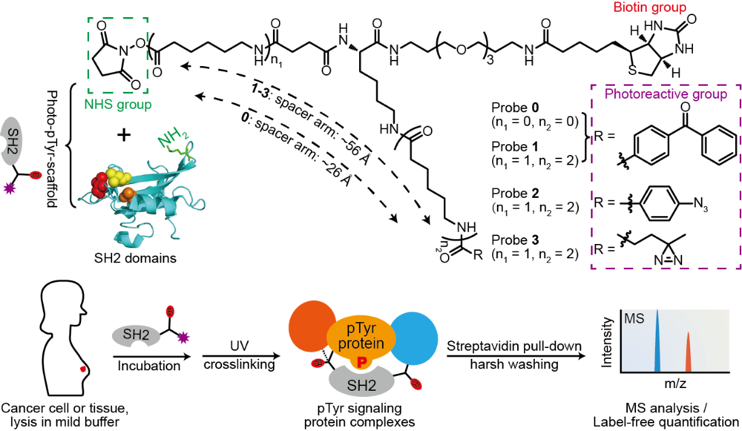
化学蛋白质组学技术Photo-pTyr-scaffold原理流程图
利用该化学蛋白质组学技术,团队成功地实现了针对人乳腺癌肿瘤样本中酪氨酸磷酸化蛋白及其复合物的高选择性富集和规模化蛋白质组学分析。与传统的免疫组化技术相比,该技术将重要药物靶点蛋白Her2的检测灵敏度提高了约100倍,有望更为精准地指导靶向性抗癌药赫赛汀(Herceptin)的临床使用。更为重要的是,该技术发现了一种针对Her2表达阴性的乳腺癌病人的潜在的新药物靶点PDGFRB。乳腺癌动物模型实验结果表明,该药物靶点的抑制可以显著地抑制乳腺癌肿瘤生长。总之,该化学蛋白质组学研究策略有望为新一代癌症药物靶点蛋白和生物标记物的规模化发现提供帮助。

高分辨生物质谱仪照片
这项研究是田瑞军团队继2015年PNAS文章、2018年Analytical Chemistry文章之后又一篇面向癌症精准医学的分析方法学和应用研究。该项目的开展得到了国家重点研发计划蛋白质机器专项子课题、国家自然科学基金面上项目、广东省自然科学基金团队项目和深圳市科创委学科布局项目等的经费支持;深圳市人民医院为研究提供了相关的临床样品和分析。

田瑞军和学生讨论问题
相关论文链接:
http://www.pnas.org/content/early/2018/09/05/1805633115
http://www.pnas.org/content/112/13/E1594.long
https://pubs.acs.org/doi/10.1021/acs.analchem.8b00596
延伸访谈:
记者:化学蛋白质组学是一门有机地结合化学生物学技术和蛋白质组学分析技术的交叉学科,您认为这门学科的前景如何,作为交叉学科有哪些优势?
田瑞军:由于很多重要的临床生物标志物都是蛋白质,而几乎所有的药物靶点均为蛋白质,化学蛋白质组学技术在生物医药和精准医学研究领域具有广阔地应用,将为创新药物研发和生物标志物组合发现提供高质量的蛋白质组学大数据支持。
作为一门化学、生物学及组学高度交叉的学科,化学蛋白质组学可以提供优于单一学科方法学的分析选择性、分析通量和分析灵敏度等。
记者:这项研究成果发布后,未来可能会对癌症的治疗与预防起到怎样的推动作用?
田瑞军:本项目研发了面向癌症精准诊疗及靶向药物开发领域的具有自主知识产权的化学蛋白质组学技术Photo-pTyr-scaffold。该技术具有高度的通用性,可以用于任何癌症样品中的信号转导相关的潜在药物靶点蛋白和生物标志物的规模化定量分析。以乳腺癌的精准治疗为例,Photo-pTyr-scaffold技术可以精准的检测一线临床靶向性抗体药赫赛汀(Herceptin)的靶点蛋白表达水平,具有高于目前临床金标准免疫组化分析约100倍的灵敏度,从而可能更为精准地指导赫赛汀的临床用药,使更多的潜在的乳腺癌患者受益。
记者:文中提到了动物模型实验,想问一下动物模型实验的优势和劣势在哪里?
田瑞军:创新抗癌药物研发一般都要经过基于动物模型的临床前体内验证阶段。相比基于模型细胞器的实验而言,动物模型可提供重要的药物体内实验依据,为临床实验奠定基础。动物模型实验的劣势往往在于所采用的动物模型不能完全模拟药物在人体内的实际作用情况。因此,在本研究中我们采用了原发性乳腺癌小鼠模型,最大程度上避免了动物模型的弊端。
记者:这一研究工作主要由您的课题组博士后初碧珠和研究助理何岸(共同第一作者)完成,想问一下您在指导学生做科研和带领团队方面有哪些心得体会?
田瑞军:我们从事的交叉科学研究具有很强的挑战性,学生需要学习化学、生物学和医学等多个领域的实验技术,更为重要的是要对所从事的癌症精准医学研究怀有极强的社会责任感和探索欲。团队成员和学生均对上述理念具有高度的认同感和联合攻关意识,从而能够在短短三年时间完成这一深度交叉的科学研究。

实验照片
供稿:化学系
采访:童小晋
照片:张晓燕




