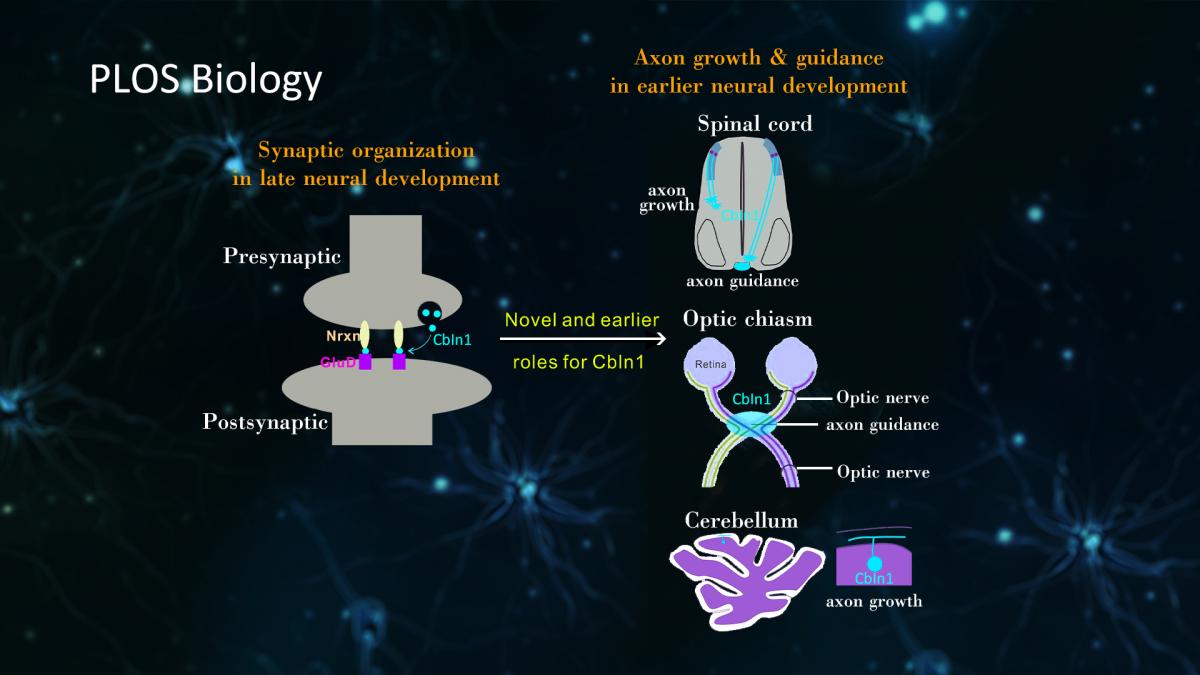
近日,南方科技大学生命科学学院副教授姬生健课题组在学术期刊PLOS Biology上在线发表了题为“Cbln1 regulates axon growth and guidance in multiple neural regions”(Cbln1在多个脑区调控轴突生长和导向)的研究论文。该研究发现突触组织者(synaptic organizer)蛋白Cbln1在神经发育早期即开始表达和发挥作用,调控胚胎期脊髓背侧连合神经元以及其它脑区神经元的轴突生长和导向。
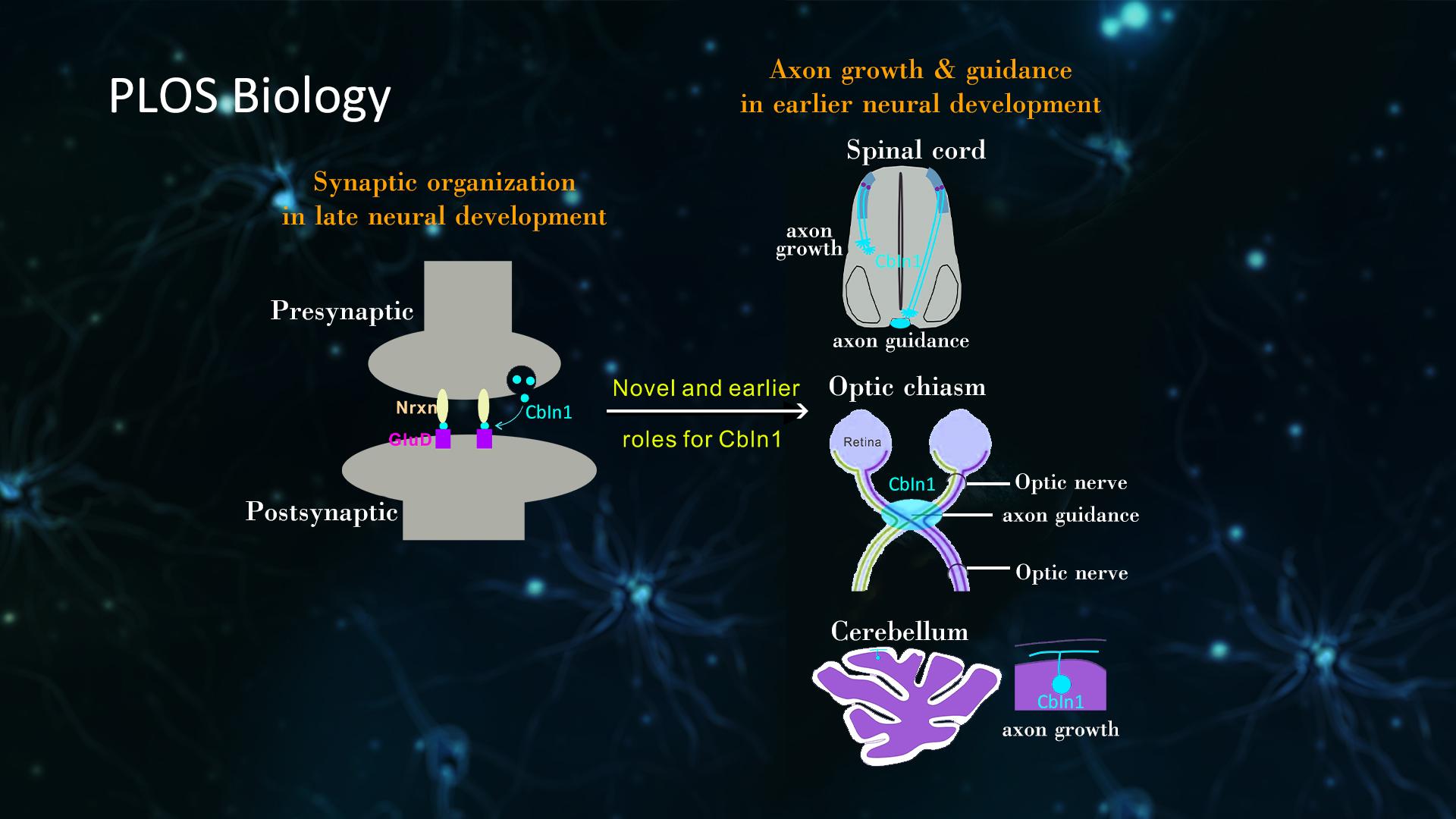 Cerebellin(Cbln)家族成员是一类分泌性蛋白,可以桥接突触前后膜受体参与突触形成。小脑中颗粒细胞和浦肯野细胞的突触形成需要Cbln1连接Nrxn和GluD;Cbln1敲除后会导致小脑中突触数量下降,进而导致小鼠运动能力下降。但是对于Cbln是否在神经发育早期表达和发挥作用则一直不清楚。
Cerebellin(Cbln)家族成员是一类分泌性蛋白,可以桥接突触前后膜受体参与突触形成。小脑中颗粒细胞和浦肯野细胞的突触形成需要Cbln1连接Nrxn和GluD;Cbln1敲除后会导致小脑中突触数量下降,进而导致小鼠运动能力下降。但是对于Cbln是否在神经发育早期表达和发挥作用则一直不清楚。
神经元轴突在轴突生长和导向因子的调控下到达靶向区域,和突触后神经元形成正确的连接,进而构建完整的神经环路。多年来的研究发现了多种发挥吸引或排斥功能的轴突导向因子,但对是否还存在新的轴突导向因子还不清楚。
姬生健在Weill Cornell工作期间进行的早期筛选发现突触组织者蛋白Cbln1在小鼠胚胎期脊髓背侧连合神经元和脊髓底板中均表达。姬生健课题组首先通过体外培养发现添加Cbln1重组蛋白能显著地促进神经元轴突的生长,说明Cbln1不止参与突触形成,还会影响神经元轴突的发育。基于这个发现,他们进一步构建了几个条件性敲除小鼠进行验证。
脊髓背侧连合神经元中特异性敲除Cbln1会导致其轴突生长缓慢,说明Cbln1可以通过自分泌途径调控神经元轴突生长。同时他们通过原位杂交技术检测了Cbln1受体在脊髓内的表达,发现只有Nrxn2在连合神经元中表达。在体外培养的脊髓背侧连合神经元中敲低Nrxn2的表达同样会抑制其轴突的生长,说明Cbln1通过受体Nrxn2调控脊髓背侧神经元轴突的生长。脊髓底板同样表达Cbln1,该旁分泌途径会不会和轴突导向因子一样发挥功能?他们接着在脊髓底板中特异性敲除Cbln1,发现脊髓背侧连合神经元轴突到达底板的进程受阻,穿越底板的神经元轴突束厚度下降,同时轴突转向点偏移中心线。他们进一步发现敲低脊髓背侧连合神经元中的Nrxn2后,外源Cbln1对轴突的吸引能力也下降。这些结果表明脊髓底板处的Cbln1通过受体Nrxn2调控脊髓背侧神经元轴突的导向。进一步研究发现,Cbln1在出生后的小脑内开始表达并且影响颗粒细胞的轴突生长。另外,Cbln1在视神经交叉处表达,在眼球向脑区投射过程中发挥导向功能。
本研究证明了神经发育后期的突触形成蛋白在神经发育早期就开始表达并发挥功能,为神经发育领域提供了新的研究思路。
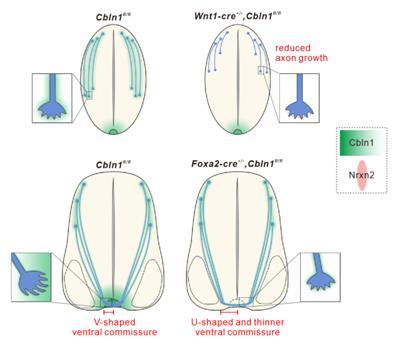
图1.Cbln1调控脊髓背侧连合神经元轴突生长和导向的工作模型
PLOS Biology期刊专门为本论文配发了Primer来进行重点推介。
姬生健课题组高级研究助理韩鹏和南科大生命科学学院博士生佘元初为论文的共同第一作者,南科大为论文第一单位。生命科学学院硕士生杨卓轩和博士后庄梦茹等也作出了重要贡献,多位实验室前成员为推进这一历时10年的课题也作出了贡献。姬生健与康奈尔大学Weill医学院教授Samie R. Jaffrey为论文共同通讯作者。
本研究得到了国家自然科学基金、深港脑科学创新研究院、深圳市基因调控与系统生物学重点实验室和美国国立卫生研究院的支持。
论文链接:https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3001853
Primer链接:https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3001880
供稿:生命科学学院
通讯员:韩鹏、付文卿
主图:丘妍
编辑:朱增光




