近日,国际著名医学期刊《Autophagy》在线发表了由南科大医学院副教授陈国安主导、国内外多家单位共同参与完成的研究论文,揭示了环状RNA circHIPH3在肺癌中的作用及调控自噬通路的新机制。
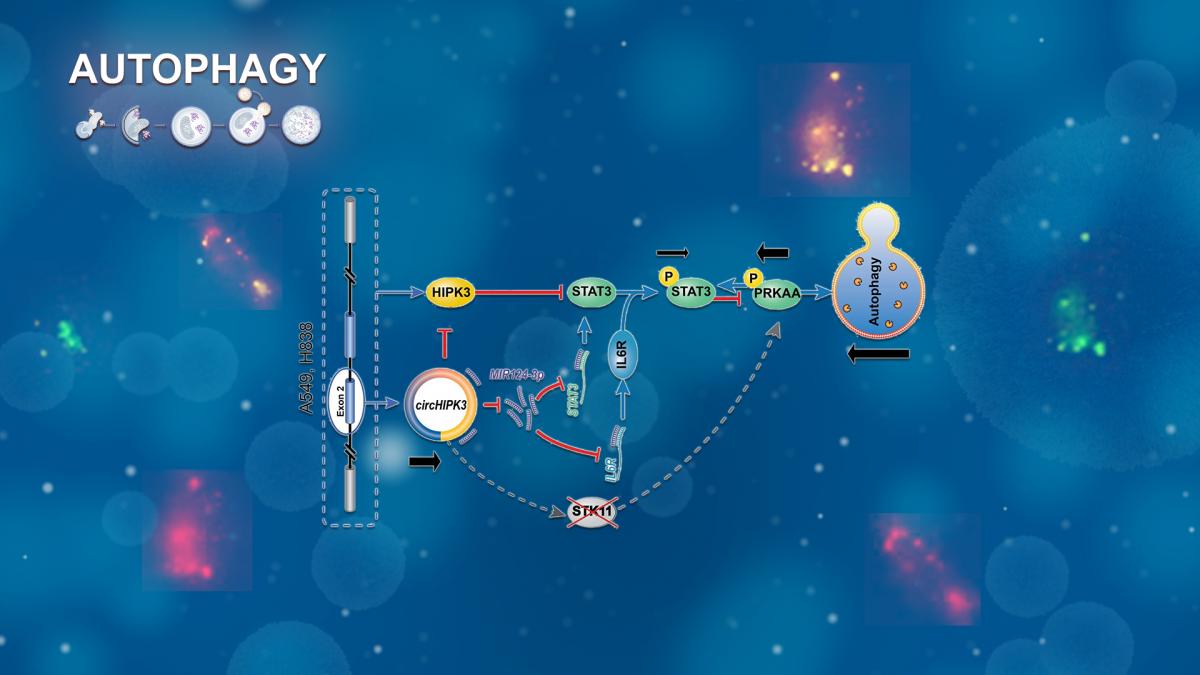
环状RNA在肿瘤治疗研究中的作用正在日益显现。近期,在多种肿瘤的HIPK3基因中存在的环状RNA(circHIPK3)被发现在肿瘤生长中起到重要作用,但其在肺癌中的作用尚未被阐明。此次的研究成果显示,沉默circHIPK3可以显著抑制肺癌细胞增殖、侵袭和转移,并导致细胞出现自噬。
在机制层面,本研究揭示出circHIPK3在STK11突变细胞系(A549和H838)中通过调控MIR124-3p-STAT3-PRKAA/AMPKa通路诱导自噬的发生。沉默STAT3或敲入MIR124-3p mimic均可重现自噬诱导。
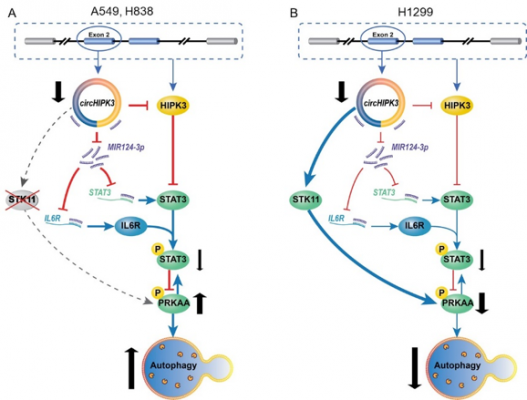 circHIPK3调控细胞自噬机制模型:(A) 在STK11基因突变的细胞,A549 和H838, circHIPK3敲低导致自噬增加主要是通过降低磷酸化STAT3和磷酸化PRKAA;(B) 在STK11基因野生型细胞,H1299, circHIPK3 敲低导致自噬减少主要是通过降低STK11-pPRKAA通路
circHIPK3调控细胞自噬机制模型:(A) 在STK11基因突变的细胞,A549 和H838, circHIPK3敲低导致自噬增加主要是通过降低磷酸化STAT3和磷酸化PRKAA;(B) 在STK11基因野生型细胞,H1299, circHIPK3 敲低导致自噬减少主要是通过降低STK11-pPRKAA通路
另外,研究团队还发现circHIPK3和linHIPK3在自噬调控中呈拮抗作用。因此,circHIPK3和linHIPK3的比例(C:L比)可能反映了肿瘤细胞中的自噬强度。团队还发现,C:L比高(>0.49)提示预后不良,且这一趋势在进展期非小细胞肺癌中更为显著。
上述结果证明,circHIPK3在部分肺癌中是自噬调控的关键分子。作为肺癌的癌基因和自噬调控基因,circHIPK3可能进一步成为预后标志甚至具有潜在的治疗价值。
陈国安说,研究中的一大困难是近期受到重视的环状RNA在肺癌中的表达谱鲜有报道,而团队也无环状RNA数据库。团队在有限的数据库中,测试了40余个环状RNA,选择了表达量与其线性母基因HIPK3几乎一样的circHIPK3做为初步的功能和机制研究对象。环状RNA研究的另一瓶颈是过表达克隆的低表达量,这可能与其复杂的成环机制有关。此外,环状RNA是否成为新的肿瘤标记物及治疗靶点还有待继续探索。
北京大学人民医院博士陈修远为第一作者,北京大学医学部教授王俊为共同通讯作者,共同参与的单位还有美国密歇根大学医学院,新疆医科大学附属医院,广东医科大学附属医院和西安交通大学第一、第二附属医院。该项研究得到了美国国立卫生院癌症研究所(NIH/NCI),密歇根大学癌症中心和外科系以及中国国家留学基金委(CSC)的支持。
论文链接:
https://www.ncbi.nlm.nih.gov/pubmed/31232177
供稿:医学院
编辑:刘馨




